 На сегодняшний день существует много различных способов лечения рака. Некоторых из них менее известных, чем химиотерапия, лучевая терапия, и хирургические операции.
На сегодняшний день существует много различных способов лечения рака. Некоторых из них менее известных, чем химиотерапия, лучевая терапия, и хирургические операции.

Генотерапия
Как известно, генные мутации могут привести к неправильному функционированию генов и бесконтрольному росту клеток. Результатом этого может стать развитие рака. (Следует, однако, помнить, что рак развивается не так просто; вероятно, для этого требуется сложная серия множественных мутаций). Эти мутации могут быть вызваны курением, факторами окружающей среды, или быть унаследованными. Основная идея генотерапии заключатся в том, что исправление этих мутаций даст нам возможность остановить рак. Сегодня разрабатывается несколько способов получения такого результата:
- Замещение нехватающих или нефункционирующих генов. Например, ген р53 называется геном подавления опухоли - название отражает его функцию. Клетки, в которых из-за мутаций этот ген отсутствует, можно «починить», помещая в них функциональные копии р53.
- Онкогены - это мутировавшие гены, которые могут или вызывать развитие новых раковых опухолей, или распространять на весь организм уже существующий рак. Нарушая активность этих генов, генотерапия сможет прекратить развитие или распространение рака.
- Использование собственной иммунной системы организма путем помещения в раковые клетки генов, которые заставят иммунную систему атаковать раковые клетки как инородные организмы.
- Введение в раковые клетки генов, которые сделают их более восприимчивыми к другим методам лечения или предотвратят развитие резистентности к ним.
- Создание «генов-смертников», которые будут проникать в раковые клетки, вызывая их саморазрушение.
- Использование генов для предотвращения образования кровеносных сосудов в раковых опухолях. Это обречет опухоль на настоящую голодную смерть в отсутствие необходимых для ее развития питательных веществ.
- Применение генов в целях защиты здоровых клеток от возникновения побочных эффектов таких методов лечения, как радиотерапия и лучевая терапия.

Как проводится
Доставка генов в нужно место - одна из самых больших трудностей и важнейших задач генотерапии. Разумеется, сделать инъекцию генов в клетки не представляется возможным, поэтому необходим некий носитель, который сможет доставить их по назначению. Обычно в качестве такого транспортного средства используются вирусы - такие же вирусы, как те, что вызывают простуду, но - деактивированные, так что они уже не могут вызвать у пациента какое-либо заболевание. Во-первых, в эти вирусы необходимо внедрить определенные гены.
После этого в некоторых случаях у пациента берут образцы клеток и в лаборатории подвергают их воздействию вируса. Вирус с необходимым геном взаимодействует с клетками, которые в течение некоторого времени растут в лабораторных условиях, а затем вводятся пациенту внутривенно, в определенные органы (например, в легкие), или непосредственно в печень. В других случаях вирусы (теперь они называются векторами) с внедренными в них генами вводят в организм пациента и они находят клетки, к которым применяется генотерапия. Достигнув целевой клетки, ген должен попасть в ее ядро и внедриться в генетический материал человека. Затем ген должен активироваться и начать вырабатывать белковые продукты, на синтез которых он и рассчитан. Если белок функционирует нормально, доставка гена в клетку считается успешной.
Генная терапия пока - совсем новый способ лечения рака, ее различные методы только проходят клинические испытания и о побочных эффектах, особенно долговременных, известно немного. О некоторых последствиях этой терапии пока можно лишь строить теории, однако генотерапия развивается быстро и может быть источником надежды для многих больных.

Биологическая терапия
Биологическая терапия помогает иммунной системе функционировать лучше благодаря использованию субстанций, которые в норме присутствуют в организме. Терапия может стимулировать организм вырабатывать больше таких субстанций, или же в ходе терапии в организм пациента вводят искусственные аналоги этих субстанций.
В биологической терапии используются: бацилла Кальметта-Герена - для лечения рака мочевого пузыряМочевой пузырь - строение и функции на ранней стадии, интерлейкин-2 - при некоторых видах меланомы и рака почкиРак почки: на ранних стадиях прогноз благоприятный
на ранней стадии, интерлейкин-2 - при некоторых видах меланомы и рака почкиРак почки: на ранних стадиях прогноз благоприятный , ритуксан (ритуксимаб) - при неходжкинской лимфоме, герцептин (трастузумаб) для лечения рака молочной железы, и многие другие препараты.
, ритуксан (ритуксимаб) - при неходжкинской лимфоме, герцептин (трастузумаб) для лечения рака молочной железы, и многие другие препараты.
Задача биологической терапии - усилить естественные защитные механизмы организма. Пока не вполне ясно, как именно работают средства биологической терапии, но очевидно, что они могут замедлить развитие рака, а также помогают иммунной системе уничтожать раковые клетки. Биологическую терапию также применяют для ослабления побочных эффектов химиотерапии и радиотерапииРадиотерапия в лечении рака: облучение в помощь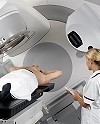 .
.
Средства для биологической терапии вводят внутривенно, подкожно, внутримышечно, или принимают перорально - в зависимости от типа препарата и заболевания, для лечения которого он используется.
Несмотря на то, что в ходе лечения используются природные или аналогичные природным вещества, они могут вызвать различные побочные эффекты, такие как лихорадка, мышечные боли и боли в суставахБоли в суставах - как разобраться что происходит? , тошнота и/или рвота, отсутствие аппетита и сильная усталость. Впрочем, большинство побочных эффектов ослабевают в течение 24-48 часов после начала лечения - примерно столько времени необходимо, чтобы привыкнуть к изменению в работе иммунной системы.
, тошнота и/или рвота, отсутствие аппетита и сильная усталость. Впрочем, большинство побочных эффектов ослабевают в течение 24-48 часов после начала лечения - примерно столько времени необходимо, чтобы привыкнуть к изменению в работе иммунной системы.

Клинические испытания
Клинические испытания тоже можно рассматривать как способ лечения рака.
Для принятия решения об участии в испытаниях может быть много причин. Часто клинические испытания являются возможностью получить доступ к методам лечения, которые не доступны при других условиях. В настоящее время, однако, лишь очень небольшое число пациентов принимают участие в клинических испытаниях - прежде всего это связано, конечно, со страхом перед новыми методами лечения.

Фазы клинических испытаний
- 1 фаза. На этом этапе идет определение идеальной дозы препарата и выявление его побочных эффектов. В первой фазе клинических испытаний участвует небольшая группа пациентов, как правило, с раковыми заболеваниями на поздних стадиях, устойчивыми к широко используемым методам лечения. В ходе испытаний используют формат постепенного повышения дозы. Если первая группа хорошо перенесла определенную дозу препарата, следующей группе дают более высокую дозу - и так далее, пока не будет определена максимальная безопасная доза.
- 2 фаза. Во второй фазе клинических испытаний оценивается эффективность тестируемого способа лечения и продолжается наблюдение за его переносимостью. На этом этапе в исследовании участвует больше пациентов.
- 3 фаза посвящена сравнению экспериментального метода лечения со стандартными методами и оценке результатов использования первого. В этой фазе клинических испытаний могут принимать участие сотни или тысячи пациентов.
- 4 фаза проходит после одобрения тестируемого метода лечения. Оно уже начало использоваться в широкой практике, но ученые продолжают заниматься повышением его безопасности и эффективности.
Желающим принимать участие в клинических испытаниях, как правило, следует самостоятельно искать информацию о таких возможностях. Следует учесть, что в исследовательских центрах существуют строгие критерии отбора для участников испытаний.
До начала испытания пациент должен получить подробную информацию о его сути и ходе испытания, и подписать соответствующий документ. После начала испытания пациент может в любой момент отказаться от дальнейшего участия.
Конечно, в большинстве случаев участие в клинических испытаниях рассматривается как крайний способ лечения рака, однако, учитывая быстрое развитие методов лечения, нельзя исключать вероятность того, что он окажется эффективным.